近日,全球腫瘤學界矚目的2025年歐洲腫瘤內科學會年會在德國柏林隆重召開。作為腫瘤領域最具影響力的國際學術盛會之一,ESMO大會每年都會公布多項可能改變臨床實踐的重磅研究。在本屆大會上,由復旦大學附屬中山醫院劉天舒教授、安徽醫科大學第一附屬醫院孫倍成教授牽頭,安科生物“HuA21注射液聯合曲妥珠單抗和化療治療HER2陽性晚期胃/胃食管交界處腺癌的Ib/II期研究”以壁報形式公布最新數據。研究階段性結果顯示,HuA21聯合療法展現出優異的抗腫瘤活性和良好的安全性,30 mg/kg劑量組客觀緩解率(ORR)80.8%,20 mg/kg劑量組客觀緩解率(ORR)76.7%,展現了其在HER2陽性晚期胃癌治療領域的巨大潛力。

HuA21注射液(重組抗HER2人源化HuA21單克隆抗體注射液)是由安科生物自主研發的I類創新藥。作為一種新型抗HER2單克隆抗體,HuA21含有與曲妥珠單抗和帕妥珠單抗完全不同的氨基酸序列,具有完全自主知識產權。其通過與現有療法不同的作用機制——靶向HER2受體亞結構域I/II,阻斷異源二聚化,并與曲妥珠單抗產生協同增效作用,臨床前研究顯示其具有較低的心臟毒性風險。
本研究是一項Ib/II期劑量遞增與擴展臨床試驗,旨在評估HuA21(20/30 mg/kg)聯合曲妥珠單抗及XELOX化療方案,用于治療HER2陽性晚期胃/胃食管交界處腺癌的安全性、耐受性及初步療效。
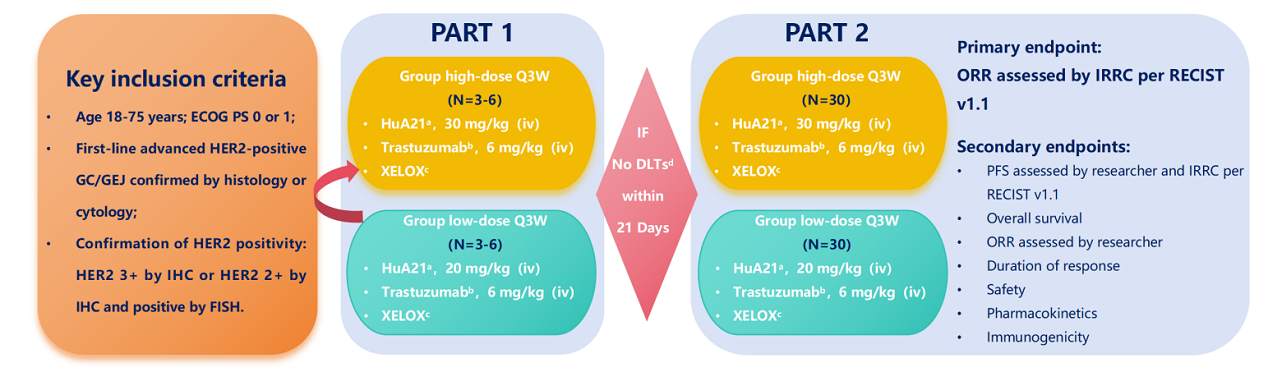
截至2025年2月20日,該研究共入組60例一線患者。經獨立影像評估委員會(IRRC)評估的關鍵結果顯示:
●有效性突出:HuA21 30 mg/kg劑量組的客觀緩解率(ORR)達到80.8%,疾病控制率(DCR)高達96.3%,20 mg/kg劑量組的客觀緩解率(ORR)達到76.7%,疾病控制率(DCR)高達100%,顯示出強大的腫瘤殺傷能力。
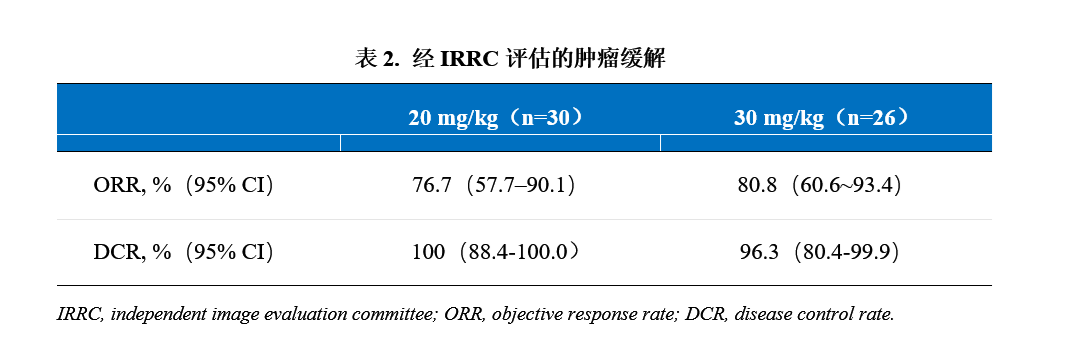
●安全性優異:HuA21 30 mg/kg劑量組和20 mg/kg劑量組安全性總體優異,治療中出現的不良事件(TEAE) 主要為 1-2 級,常見的TEAE為血小板計數降低、貧血、中性粒細胞計數降低、白細胞計數降低、天冬氨酸轉氨酶升高。30 mg/kg劑量組的表現優于20 mg/kg劑量組,整體安全性可控,未出現非預期安全信號。基于更優的獲益-風險特征,本研究推薦HuA21 30 mg/kg作為后續III期臨床研究劑量。
本次ESMO大會首次對外公開HuA21注射液優異的臨床數據,標志著這款國產創新藥向著成功上市、造福患者的目標邁出了堅實的一步,是安科生物在腫瘤創新藥領域的重要里程碑。未來,安科生物將持續推進HuA21的后續臨床研究進程,并探索其在更多HER2陽性腫瘤中的應用潛力,早日實現臨床價值,為全球患者提供更多、更好的治療選擇。
轉自:新浪財經


【版權及免責聲明】凡本網所屬版權作品,轉載時須獲得授權并注明來源“中國產業經濟信息網”,違者本網將保留追究其相關法律責任的權力。凡轉載文章及企業宣傳資訊,僅代表作者個人觀點,不代表本網觀點和立場。版權事宜請聯系:010-65363056。
延伸閱讀