2025年7月底,多倫多阿爾茨海默病協會國際會議(AAIC)上,阿爾茨海默病協會 (AA) 聯合綜合指南小組,投下一枚重磅“炸彈”——史上首份阿爾茨海默病(AD)血液生物標志物(BBM)臨床實踐指南 (CPG) 正式發布(下稱“指南”)。這并非一次簡單的學術更新,而是一個新時代的開端,標志著AD血液檢測,從實驗室的研究工具,正式加冕為擁有官方背書的AD臨床診斷標準。
對于產品開發者、學術研究者以及所有致力于攻克AD難題的IVD從業者而言,這意味著什么?菲鵬看到了這份指南直擊的深刻的市場變革將帶來的戰略意義、商業價值,以及對客戶和社會發展的長遠利益:
市場被激活。過往“模糊不清”的臨床路徑,如今有了清晰的“指南針”。血液檢測被正式納入專科診斷流程,為二級、三級醫療機構的記憶門診提供了明確指引。臨床上量“起勢”已經到來。
支付可預期。有了權威機構指南背書,進入醫保支付的進程無疑將大大加速。一個真正意義上由臨床需求驅動的龐大市場正悄然拉開序幕。
機遇與鐵律:指南設下的“雙90”挑戰
指南對產品的臨床性能給出了明確的量化要求,據此將其清晰劃入兩個賽道:
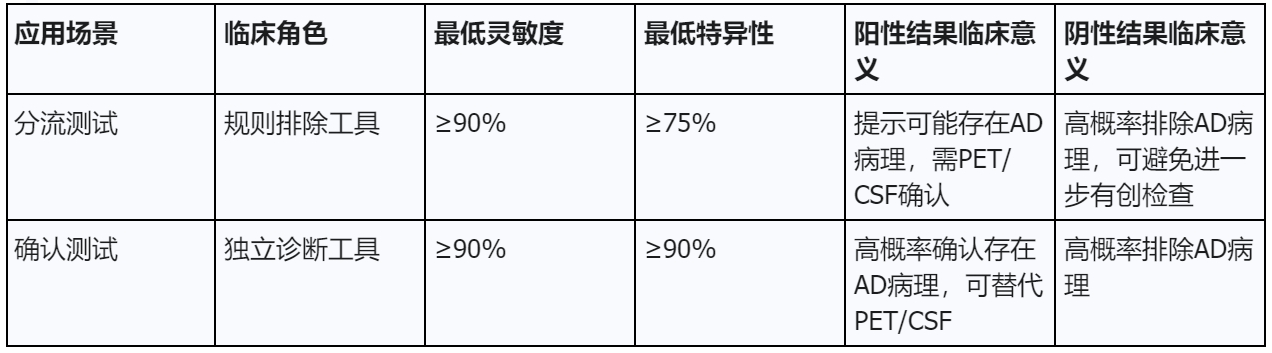
表1:AAIC 2025 AD血液生物標志物指南:關鍵性能要求與應用場景
分診賽道:靈敏度≥90%,特異性 ≥75% 的測試,可作為高效的分流工具。
確診賽道:靈敏度≥90%,特異性 ≥90% 的測試,可作為金標準PET或腦脊液檢測的替代方案。
“雙90”這個數字組合,將成為未來幾年所有AD診斷產品開發者繞不開的“珠穆朗瑪”。
與此同時,行業銳評也指出了殘酷現實:
證據確定性低:指南制定小組坦言,現有研究證據的總體確定性“低到極低”,超過300項研究因數據質量不佳被排除。這說明,市面上絕大多數產品距離指南的要求,還有很長的路要走。
商業化亂象:指南明確警告,商業化測試質量參差不齊,缺乏嚴格監管。
研發迭代困境:“雙90”的達成不是簡單優化,而是系統工程。它要求從最源頭的原料設計、項目設計(如“雙截斷值”(Dual-Cutoff)應用),到大規模、高質量的真實世界數據驗證,進行全面革新。
挑戰暗藏機遇——誰能率先拿出經過嚴格驗證符合指南高標準的產品,誰就能定義市場,建立信任。
“指南針”已指明黃金航向。面對密布“技術暗礁”的航道,如何突圍?
破局之道:以卓越原料與系統方案決勝“雙90”
前瞻性檢測設計:“雙截斷值”策略
一個源于專家共識的、更精妙的技術建議是采用 “雙截斷值”(Dual-Cutoff) 策略。該設計不設單一閾值,而是創建了三個明確區間:
明確陽性區: AD病理可能性極高;
明確陰性區: AD病理可能性極低;
中間/待定區(3%~15%): 結果不確定,需進行后續確認性檢測。
這種將3%~15%的患者置于中間地帶的方法,并非缺陷,而是一種特性。它在統計學上更穩健地承認了健康人群與患病人群間的生物學重疊,為臨床醫生管理不確定性提供了框架,從而極大降低了因單一臨界值而導致的誤診風險。對于開發者而言,圍繞這一原則設計檢測產品,是技術成熟與臨床責任感的體現。
更深層次的博弈:超越實驗室的戰略要務
盡管指南在品牌上保持中立,但其所審查的證據壓倒性地指向了在蘇氨酸217位點磷酸化的tau蛋白(p-tau217),認為它是迄今最穩健、最具前景的生物標志物 。對于開發者而言,這是一個集中研發資源的明確信號——
達到技術指標只是成功的一半。新市場的真正贏家,將是那些能深刻理解指南及整個醫療生態系統背后更深層戰略邏輯的企業。
戰略要務一:“低確定性”證據是機遇,而非缺陷
指南建立在 “低確定性證據” 之上——這點看似缺陷,實則蘊含巨大戰略機遇。指南明確指出,該領域仍在“蓬勃發展”,推薦意見將隨證據的演進而定期更新。
這預示著一個動態且快速成熟的市場。當前的性能閾值是 “地板”,而非“天花板”。那些僅僅以“達標”為目標開發產品的公司,將很快面臨技術迭代的風險。最明智的策略是,以前瞻性眼光布局,開發出性能遠超當前“確認級”標準的產品,從而樹立新的行業標桿。這種“不確定性”的環境,反而為追求卓越品質和技術創新的企業創造了巨大的溢價空間。
戰略要務二:支付方的終極考驗與精準度的經濟學
目前,大多數BBM檢測尚未被醫保覆蓋,患者需承擔高昂的自付費用 。要獲得醫保(如Medicare)的準入,最關鍵的是證明其 “臨床實用性”(clinical utility)——即檢測結果能改善臨床決策并帶來更好的健康產出。
要產生成本效益或流程效益,關鍵要有過硬的產品性能。
戰略要務三:公平性指令——多元化驗證已成必要項
一個巨大的商業風險在于生物標志物在不同種族間的性能差異。越來越多的證據表明,關鍵AD生物標志物的水平在不同人群中存在顯著差異。
監管審查:FDA等監管機構日益強調健康公平。在單一、同質化人群中驗證的產品,在申請廣泛應用時可能面臨嚴峻的審批挑戰 。
市場準入:一個在某些人群中準確性打折的檢測,可能導致誤診或診療延遲 。支付方也可能因缺乏在多元化人群中表現一致的證據而拒絕給予廣泛的醫保覆蓋。
在AD診斷的新紀元,機會屬于深刻理解臨床挑戰,并提供系統性解決方案者,他們既是上游原料深度協同者,又是中游產品工程實現者及下游臨床真實數據驗證者。
決勝之基:高性能原料如何贏得競賽
上述三大市場挑戰——超越動態標準、證明臨床實用性、確保多元化性能——最終都指向了同一個根源:核心原料品質。
在血漿這樣復雜的樣本中,檢測皮克/毫升(pg/mL)甚至更低濃度的p-tau217,是一項巨大的技術挑戰。
超凡的親和力與動力學特性:能夠從海量背景蛋白中精準“捕撈”并穩定結合極其微量的靶蛋白。
極致的特異性:能精確識別p-tau217,以及與配對表位的結構特性等其他磷酸化異構體或非磷酸化tau不發生交叉反應,這是控制假陽性的根本。
優化的表位配對:捕獲抗體和檢測抗體需對標志物存在形式與來源有極強的科學理解,確保定量一致性,以構建穩定可靠的“三明治”免疫反應結構。
卓越的批間一致性:確保產品在不同生產批次間性能穩定如一,這是通過FDA、IVDR等法規審批和獲得臨床信任的基石。
菲鵬打造的AD血檢早診方案,承受住了新時代嚴苛挑戰,為開發下一代高性能AD診斷產品提供了一整套解決方案。
王牌產品:p-tau217抗體對
打造“確認級”AD診斷產品的核心引擎。該抗體對經過精心篩選和嚴格驗證,旨在滿足高難度免疫檢測對靈敏度、特異性和穩定性的極致要求。
全方位產品矩陣
菲鵬的視野不止于p-tau217。菲鵬的解決方案覆蓋AD核心標志物全譜系,涵蓋AD全病程全周期,包括Aβ42、Aβ40、其他p-tau亞型(如p-tau181)、神經絲輕鏈(NFL)等,為開發單靶標或多靶標聯檢產品提供全面支持。
質量承諾
對于IVD開發者而言,原料的穩定性、可靠性是生命線。菲鵬擁有規模化的生產能力和嚴格的質量管理體系,確保卓越的批間一致性,為產品的研發、注冊和商業化全程保駕護航。
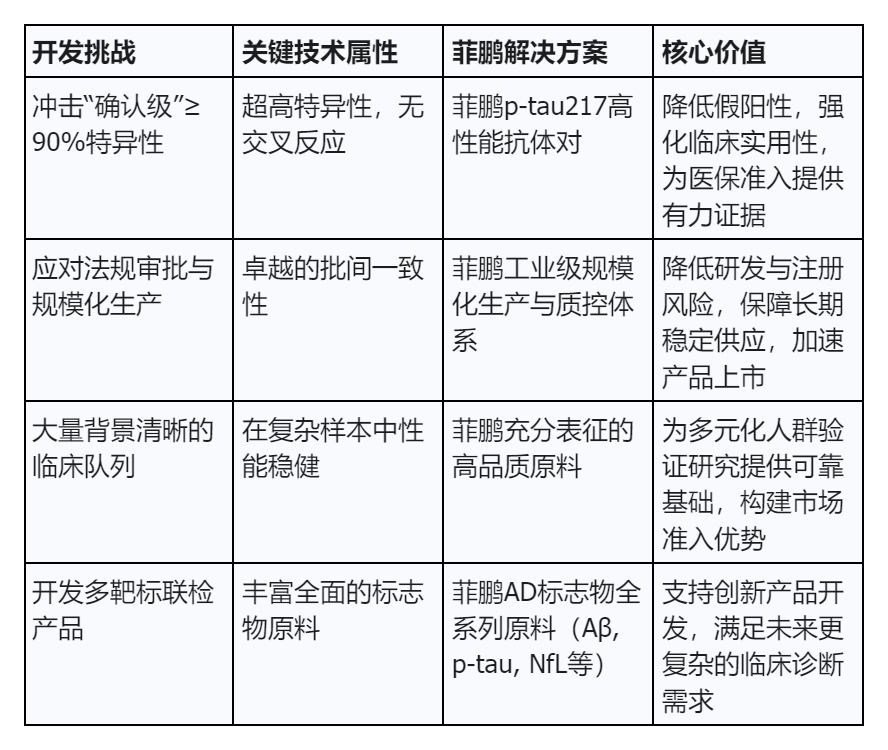
表2:菲鵬AD解決方案,助力應對AD診斷市場挑戰
臨床效能評估:
菲鵬p-tau217 試劑與臨床診斷的結果相比較,ROC 曲線及樣本濃度分布如下圖所示,AUC>0.90,按照截斷值 1.04pg/mL, 臨床敏感性為 91.84%(86.27%~95.27%),特異性為 94.40%(90.65%~96.70%)。陽性預測值(PPV)為 90.07%,陰性預測值(NPV)為 94.76%。
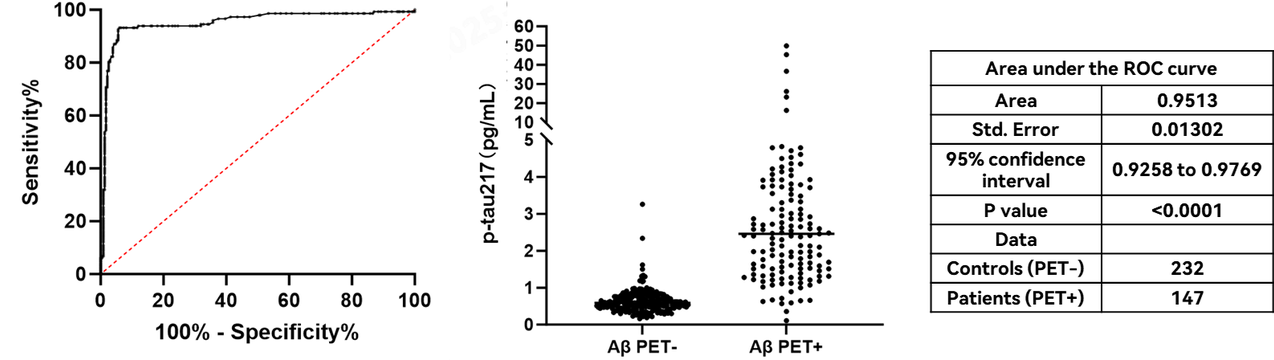
臨床效能
攜手行業:菲鵬AD血檢方案使命與價值
菲鵬認為,攻克“雙90”高地,必須回歸本源,從最核心的原料與解決方案入手,并以臨床資源加速。菲鵬AD整體解決方案首度全面推出,旨在攜手IVD行業,共同把握此次臨床上量的歷史性機遇。
這正是菲鵬血檢方案的使命與價值所在。
鎖定核心靶點,打造高性能原料
指南的背后,是對p-tau217等核心生物標志物的認可。菲鵬的AD解決方案,正是圍繞p-tau217及其比值等關鍵指標進行深度開發。菲鵬通過科學的抗原抗體設計、嚴苛的篩選與驗證流程,打造出具有卓越靈敏度與特異性的核心原料,為您的產品達到“雙90”奠定最堅實的基石。
科學項目設計,賦能產品快速迭代
菲鵬深知,高質量的原料只是第一步。如何通過科學的實驗設計以及干擾內因理解,如何建立全面的系統評估體系來應對“證據確定性低”的質疑,是產品成功的關鍵。菲鵬不僅提供原料,更提供基于大量真實世界數據迭代而來的解決方案服務,助力縮短研發周期,降本增效。
攜手并進,把握臨床機遇
指南已發布,市場窗口期轉瞬即逝。誠邀有意者,協同菲鵬帶來的AD核心原料與解決方案,設計產品開發藍圖,用經得起市場考驗的高質量產品,回應臨床迫切需求,共迎AD血液診斷市場的爆發。

菲鵬AD解決方案合作模式示意圖
附:指南對優質AD血檢產品的定義
指南由阿爾茨海默病協會召集的臨床醫生、學科專家和指南方法學家小組進行了系統綜述,以評估血液生物標志物 (BBM) 生物標志物(包括磷酸化 tau (p-tau) 變體和淀粉樣β蛋白 (Aβ) 比例)與腦脊液生物標志物、淀粉樣蛋白 PET 成像或神經病理學相比的診斷準確性。專家組采用“推薦、評估、制定和評價分級”(GRADE)方法評估證據的確定性,并采用GRADE證據到決策 (EtD) 框架制定推薦。
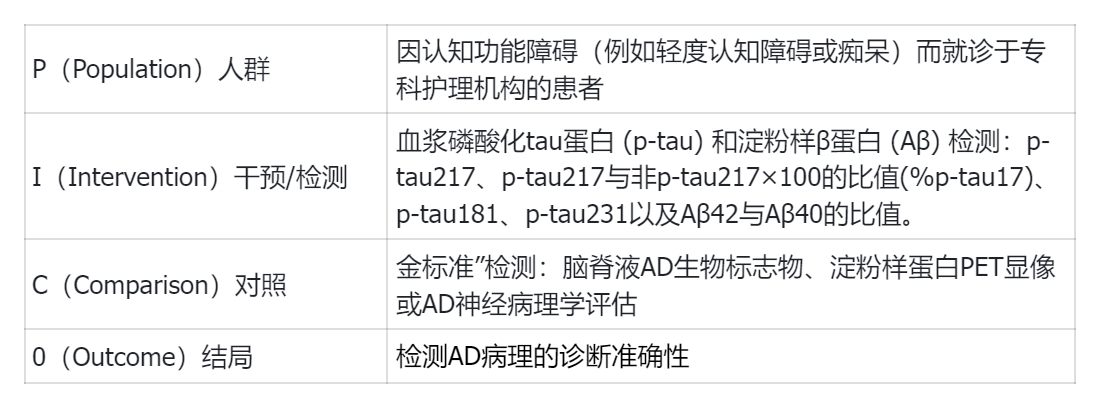
表3:血液生物標志物臨床實踐指南(BBM CPG)的PICO臨床問題框架
表4:對專門護理環境中針對客觀認知障礙患者進行淀粉樣蛋白病理檢測,使用BBM測試的建議
核心要點
專家組指出,不同廠家的測試準確性存在顯著差異,許多市售的BBM測試達不到上述閾值,尤其是使用單一截斷值的情況。
專家組提醒,在臨床實踐中,即使是很小的檢測不精密度和偏倚也會影響結果解讀,尤其是在應用固定診斷界值時。因此,臨床實驗室需要評估和監測生物標志物檢測的變異系數(CV),以確保性能的一致性,并幫助降低因分析變異性而導致的錯誤分類風險。這對于在AD病理陽性和陰性個體之間有小倍數變化的生物標志物尤其重要。
高品質AD血檢產品的要求
隨著新的臨床實踐指南的發布,對AD血液檢測產品的性能和質量有了更明確且嚴格的要求。一款優質的AD血液檢測產品,應在多方面滿足臨床及患者需求,以推動AD診斷與治療的進步。
診斷性能達標:根據指南,符合確診測試的AD血液檢測產品應具備≥90% 的靈敏度和≥90% 的特異性,以確保精準檢測出阿爾茨海默病病理,這是作為確認性檢測的關鍵指標。對于用于分診檢測的產品,靈敏度需≥90%,特異性≥75%,能夠有效排除非AD患者,減少不必要的后續檢查。
滿足臨床級技術性能要求:所有技術性能指標(精密度、準確度、靈敏度、特異性、干擾、穩定性等)都通過嚴格設計的、符合國際/國內指南(如CLSI系列文件、ISO 20916等)的研究驗證。在真實世界的實驗室環境下,面對不同樣本、不同操作員、不同批次試劑時,都能穩定輸出低變異、高準確的結果。
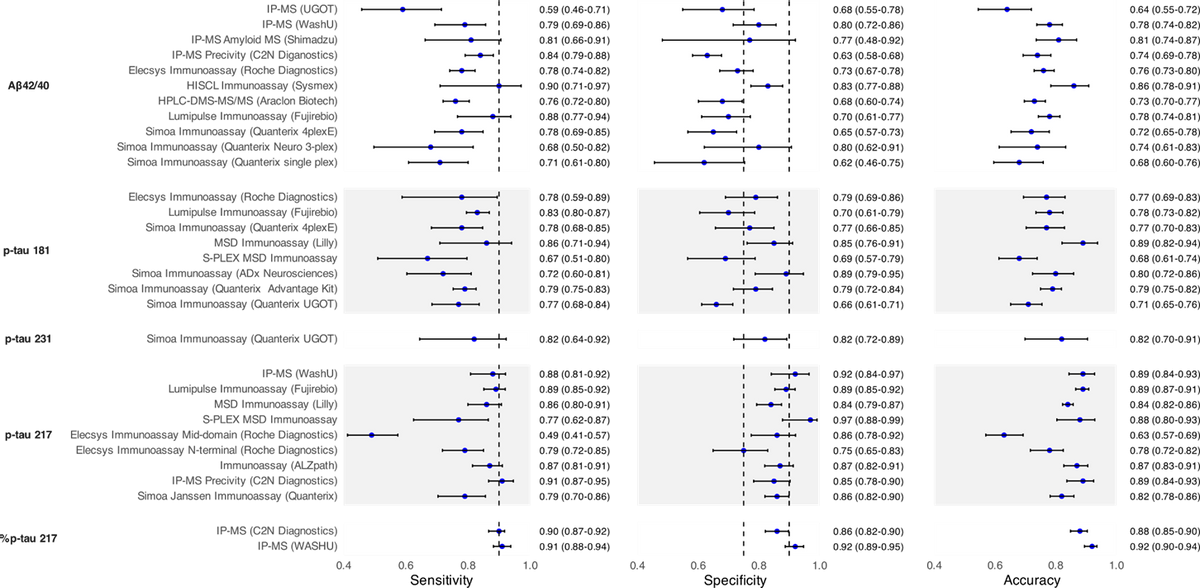
AD血檢指標示意
轉自:中國網


【版權及免責聲明】凡本網所屬版權作品,轉載時須獲得授權并注明來源“中國產業經濟信息網”,違者本網將保留追究其相關法律責任的權力。凡轉載文章及企業宣傳資訊,僅代表作者個人觀點,不代表本網觀點和立場。版權事宜請聯系:010-65363056。
延伸閱讀